14. Cálculo del flash Isotermico (T, P)¶
Se presenta una implementación del calculo del flash isotermico bifasico utilizando la ecuación de estado Peng-Robinsong (PR) [2] junto con las reglas de mezclado de Van Der Waalls [2].
El cálculo del flash isotermico bifasico es un cálculo básico en la introducción de los procesos de separación porque es el esqeuma tecnologíco de separación más simple, en el que ingresa una corriente de fluido a un «tanque» calentado por un flujo de calor en el que se obtiene una corriente de salida por cada fase presente en el sistema. En el caso bifasico, una corriente de líquido y otra de vapor, tal como se muestra en la figura 1.
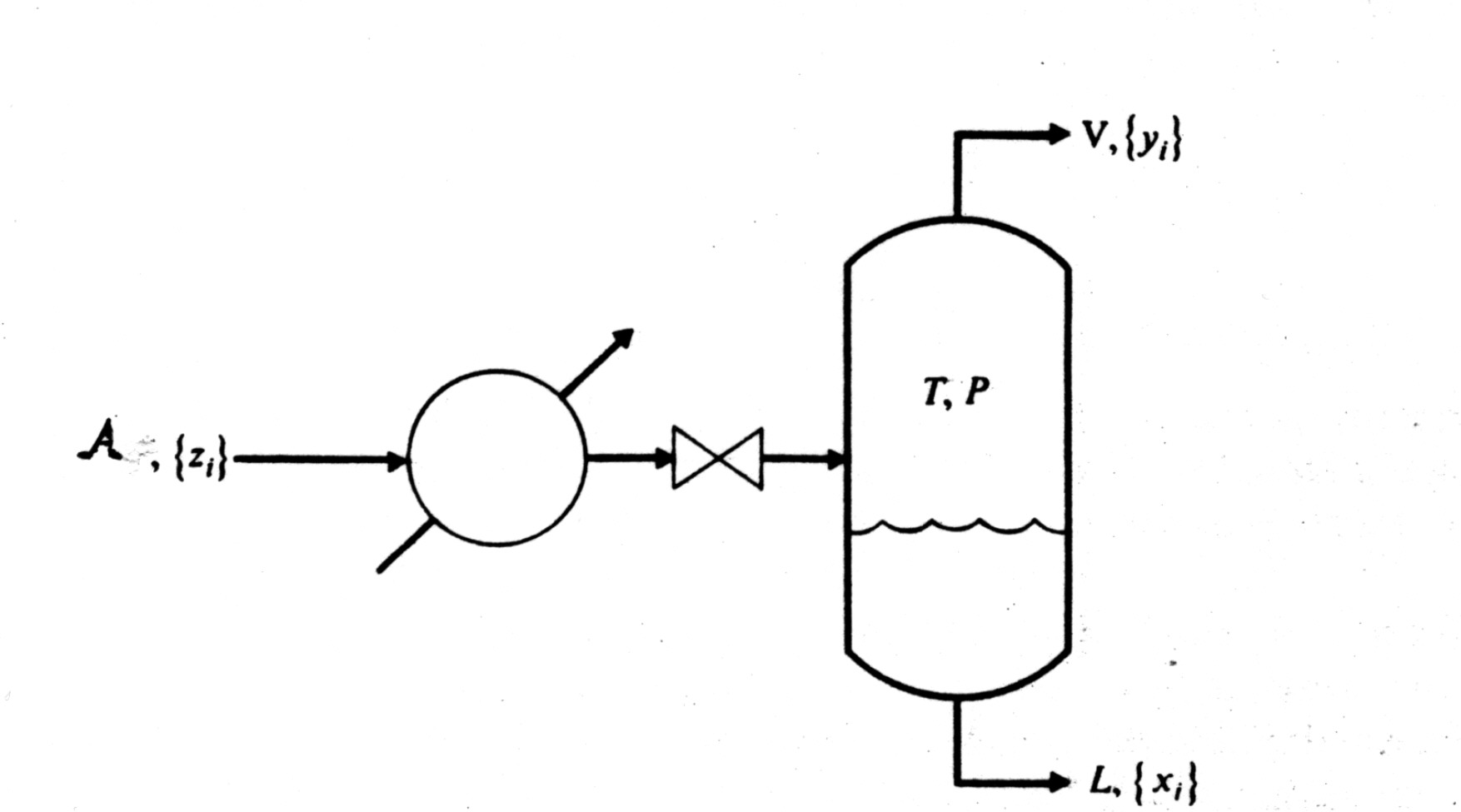
Figura 1. Esquema del cálculo del flash isotermico
14.1 Modelo flash líquido-vapor¶
El modelo del flash isotermico bifasico, corresponde al balance de materia global y por componente en el tanque separador que se muestra en la figura (1), junto con la condición de equilibrio de fases líquido-vapor.
Coeficiente de distribución 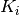
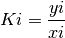
Aproximación de wilson para el coeficiente de distribución 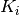
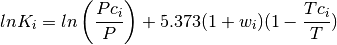
Rachford-Rice 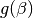
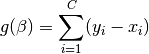
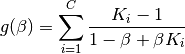
Derivada de la función Rachford-Rice 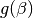
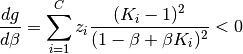
Valores límites de la función Rachford-Rice 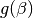
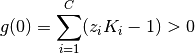
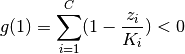
Ecuaciones para calcular las fracciones molares de cada fase
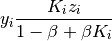
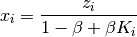
Relaciones que determinan los valores mínimos y máximos para
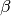
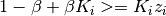
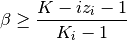
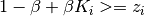
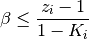
Valores extremos de la fracción de vapor en el sistema 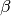
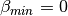
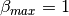
14.2 Algoritmo¶
- Especificar la Presión
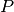 , Temperatura
, Temperatura 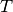 y número de
moles
y número de
moles 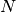 de cada componente del sistema
de cada componente del sistema - Calcular el coeficiente de distribución
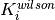 a partir
de la relación de Wilson
a partir
de la relación de Wilson - Calcular el valor de
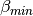
- Calcular el valor de
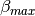
- Calcular el promedio de beta, usando Beta minimo y Beta máximo
- Resolver la ecuación de Rachford-Rice
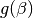 , para
calcular
, para
calcular 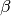 con una tolerancia de
con una tolerancia de 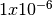
- Calcular las fracciones molares del líquido
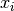 y del vapor
y del vapor
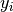
- Calcular los coeficientes de fugacidad
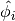 para las
fracciones molares del líquido
para las
fracciones molares del líquido 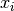 y del vapor
y del vapor 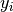
- Calcular el coeficiente de distribución
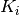 a partir de los
coeficientes de fugacidad del componente i
a partir de los
coeficientes de fugacidad del componente i 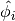
- Volver a resolver la ecuación de Rachford-Rice
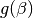 ,
para calcular
,
para calcular 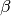 con una tolerancia de
con una tolerancia de 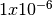
- Verificar la convergencia del sistema con una tolerancia de
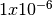 para
para 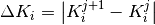 ,
siendo está situación la convergencia del procedimiento.
,
siendo está situación la convergencia del procedimiento.
14.2.1 Implementación¶
En la implementación del cálculo del flash isotermico, se tiene 3 partes importantes:
- Cálculo de los coeficientes de distribución por medio de la ecuación de Wilson
- Cálculo de los valores mínimos y máximos para la fracción
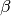
- Cálculo del step para calcular la fracción
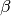
Ecuación de Wilson¶
def Ki_wilson(self):
"""Equation of wilson for to calculate the Ki(T,P)"""
variable_0 = 5.373 * (1 + self.w) * (1 - self.Tc / self.T)
lnKi = np.log(self.Pc / self.P) + variable_0
self.Ki = np.exp(lnKi)
return self.Ki
Cálculo de los valores mínimos y máximos para la fracción 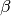 ¶
¶
def beta_initial(self):
self.Ki = self.Ki_wilson()
self.Bmin = (self.Ki * self.zi - 1) / (self.Ki - 1)
self.Bmax = (1 - self.zi) / (1 - self.Ki)
self.Binit = (np.max(self.Bmin) + np.min(self.Bmax)) / 2
return self.Binit
Cálculo del step para calcular la fracción 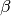 ¶
¶
def beta_newton(self):
iteration, step, tolerance = 0, 1, 1e-5
while True:
self.Binit = self.Binit - step * self.rachford_rice()[0] / self.rachford_rice()[1]
iteration += 1
while self.Binit < self.Bmin or self.Binit > self.Bmax:
step = step / 2
if abs(self.rachford_rice()[0]) <= tolerance or (iteration >= 50):
break
return self.Binit
14.3. Resultados¶
A continuación se muestran los resultados numéricos del calculo del flash isotermico bifasico para una mezcla de los componentes (C3-Ci4-C4), que corresponde al cálculo del flash isotermico propuesto por (Elliott & Lira, 2012) el ejemplo 10.7 de su libro Introductory Chemical engineering thermodynamics. En la tabla 1, se presentan las especificaciones de la presión P, temperatura T y flujo F junto con las fracciones molares del líquido, del vapor y la fracción de fase resultanten usando como modelo termodinámico la ecuación de estado Peng-robinson (PR) y las reglas de mezclado de Van Der Waalls.
En la tabla 1., se presenta el resultado del cálculo del flash
isotermico utilizando solo el 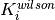
Tabla.1 flash isotermico 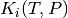 Mezcla ideal
Mezcla ideal
| Presión Bar | Temperatura K | Flujo F mol/h |
|---|---|---|
| 8 | 320 | 1 |
| Componente | 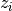 |
líquido 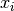 |
Vapor 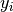 |
|---|---|---|---|
| C3 | 0.23 | 0.18357118 | 0.37209837 |
| Ci4 | 0.67 | 0.70479988 | 0.56349276 |
| C4 | 0.10 | 0.11162895 | 0.06440887 |
| función g | derivada función 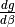 |
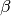 |
|---|---|---|
| 6.1017797856749434e-07 | -0.20663315922997191 | 0.24627123315157093 |
mientras que en la tabla 2, se muestra el resultado del cálculo del
flash isotermico utilizando el resultado de 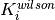 como
valor inicial para el procedimiento del cálculo del flash isotermico
incluyento el cálculo de los coeficientes de fugacidad
como
valor inicial para el procedimiento del cálculo del flash isotermico
incluyento el cálculo de los coeficientes de fugacidad
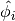 con la ecuación de estado PR.
con la ecuación de estado PR.
Tabla.2 Flash isotermico 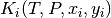 (PR)
(PR)
| función g | derivada función 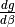 |
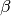 |
|---|---|---|
| -9.7482523918959729e-06 | -0.13108663002971882 | 0.19530673657 |
De esta forma, se observa que el algoritmo empleando la ecuación de estado Peng-Robinson (PR) converge en a una solución cercana de la solución que utiliza la aproximación de wilson para el coeficiente de distribución Ki, mostrando ser efieciente para casos simples como el presente en este capítulo.
14.3.1 Efecto de la temperatura y presión sobre 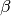 ¶
¶
Para el mismo sistema que se presentó en las tabla 1 y 2, en la figura 2
se muestra la solución del cálculo del flash isotermico para un rango de
presión y temperatura en el cual la fracción vaporizada 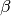 varia entre 0 y 1. En este caso, al aumentar la presión
varia entre 0 y 1. En este caso, al aumentar la presión 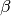 disminuye mientras que el efecto de la temperatura es el contrario.
disminuye mientras que el efecto de la temperatura es el contrario.
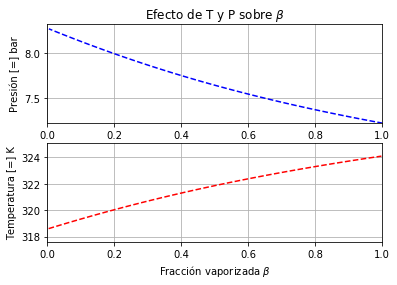
Figura 2. Efecto de la temperatura y presión sobre 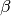
14.4 Conclusiones¶
- Se implemento el cálculo del flash isotermico bifasico utilizando la ecuación de estado Peng-Robinsong (PR) tomando las recomendaciones planteadas en el curso de termodinámica de fluidos para mejorar la convergencia del cálculo.
- Se encontró que se utilizan en promedio 3 iteraciones para calcular
el valor
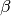 en cada paso que se mantienen constantes los
valores
en cada paso que se mantienen constantes los
valores 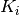 .
.
14.5 Referencias¶
- Curso de especialización en Termodinámica de fluidos. Ph.D Martín Cismondí. Marzo-Junio (2017)
- Introductory Chemical engineering thermodynamics. J. Richard Elliott , Carl T. Lira. Prentice Hall (2012)